AMINAS
Son derivados orgánicos de amoniaco con uno o más compuestos alquilo o arilo enlazados al átomo de nitrógeno.
ESTRUCTURA
FUNCIONES
1) Bioregulación
2) Neurotransmisión
3) Defensa contra depredadores
4) Drogas y medicamentos
Efectos al medio ambiente, alimentos, salud.
El principal impacto ambiental de las aminas es el contaminar el aire y la atmósfera en general.
Las aminas llegan a ser bastante tóxicas y contaminantes, sobre todo por la cantidad de carbono que pueden llegar a tener y porque el amoniaco es un elemento muy difícil de sintetizar y muy tóxico.
Una reacción muy importante de las aminas es la que tiene lugar con el ácido nitroso. El carbocatión resultante reacciona de forma descontrolada con los nucleófilos presentes en el medio (por ejemplo agua, cloruro, etc.) produciendo una mezcla de alcoholes, haluros de alquilo y también alquenos por eliminación.
Ejemplos de Aminas
Alcaloides
Se clasifican según el número de radicales alquilo o arilo unidos al átomos de nitrógeno.
PROPIEDADES FISICAS
- Las aminas son bases ligeramente fuertes, sus soluciones acuosas son básicas.
- Una amina puede abstraer un protón del agua, dando lugar a un ión amonio y a un ión hidróxido.
- La constante de basicidad esta dada por la ecuación:
Solubilidad de las aminas y las sales de amonio
La mayoría de las aminas, que contienen más de seis átomos de carbono, son relativamente insolubles en agua. En presencia de ácido diluido (en disolución acuosa), estas aminas forman las sales de amonio correspondientes, por lo que se disuelven en agua. La formación de una sal soluble es una de las características de las pruebas para el grupo funcional amina.
Una amina puede convertirse en sal de amonio mediante un tratamiento con ácido. La sal de amonio es soluble en agua. Al tratar la sal de amonio con soluciones básicas la volverá a convertir en la amina.
Cocaína.
La cocaína generalmente se consume en forma de clorhidrato. Cuando el clorhidrato de cocaína se trata con hidróxido de sodio y se extrae con éter se vuelve a transformar en la base volátil, utilizada para fumar.
La cocaína se encuentra normalmente como una sal de clorhidrato porque es sólida y se puede manejar fácilmente. Al neutralizar el clorhidrato de cocaína se convierte en una base libre que es más volátil.
NOMENCLATURA
Regla #1
Se nombra primeros los grupos alquilos unidos al Nitrógeno seguido de la palabra amina. Se pueden usar los prefijos di o tri para indicar dos o tres grupos sustituyentes iguales.
Regla #2
Estructura más complicada, se pueden nombrar llamando al grupo -NH2 como amino. El grupo amino se nombra como cualquier otro sustituyente, con un localizador que indique su posición en la cadena o anillo de átomos.
Regla #3
Elegir la cadena principal que contenga el mayor número de átomos de carbono y se la nombra sustituyendo la terminación -o del alcano por la terminación -amina. La posición del grupo amino y de los sustituyentes o cadenas laterales se indica mediante los correspondientes localizadores. Se emplea el prefijo N- para cada cadena alifática que se encuentre unido al átomo de nitrógeno.
Regla #4
Las aminas secundarias o terciarias, se nombran tomando el sustituyente más grande como cadena principal, todos los demás grupos se nombran utilizando la letra N- seguida por el nombre del sustituyente.
Ejemplos
Bases de las amidas.
Son bases fuertes. Pueden sustraer un protón del agua, formando un ión amonio y un ión hidroxilo. A la constante de equilibrio de esta reacción se le llama constante de basicidad de la amina y se representa por Kb.
- Las alquilaminas son bases más fuertes que el amoniaco.
- Esta diferencia se explica por el efecto electrón-dador de los grupos alquilo, que estabilizan la carga positiva del nitrógeno, lo que provoca una disminución de la energía potencial del catión correspondiente y desplaza el equilibrio hacia la derecha.
- De acuerdo al anterior razonamiento, se debería esperar que las aminas secundarias fuesen bases más fuertes que las aminas primarias, y las aminas terciarias fuesen bases más fuertes que las aminas secundarias. La situación real es más complicada debido a la solvatación.
Derivados Nitrogenados de los Hidrocarburos.
AMIDAS
• Se sustituye el grupo –OH de un ácido por el grupo amino –NH2 (–NHR o –NRR’ en el caso de amidas sustituidas).
• Una amida importante es la urea, que se encuentra en la orina de los mamíferos.
• Se utiliza como fertilizante y para fabricar plásticos y adhesivos.
NOMENCLATURA
Se nombran sustituyendo la terminación -oico o -ico del ácido correspondiente por -amida; o sustituyendo la terminación -o del hidrocarburo del que procede el correspondiente ácido por el sufijo -amida. Si se trata de amidas sustituidas, hay que nombrar además los radicales unidos al nitrógeno, anteponiendo la letra N.
- Amidas como grupo funcional: se nombran reemplazando el sufijo -o del alcano por -amida.
- Grupo amida unido a ciclos: en compuestos cíclicos se nombra el ciclo y se termina con el sufijo -carboxiamida.
- Amidas como sustituyentes: cuando no es grupo funcional se ordena alfabéticamente con el resto de sustituyentes utilizando el prefijo carbamoíl.
Nitrilos
• Moléculas reactivas de amplia aplicación en síntesis orgánica. Por ej, la hidrólisis de nitrilos en presencia de ácido fuerte o base fuerte da lugar a ácidos carboxílicos; la hidrogenación catalítica de nitrilos permite la preparación de aminas primarias.
• La cafeína, la nicotina, la morfina, forman una clase muy importante de aminas que se produce en algunos vegetales.
Nomenclatura:
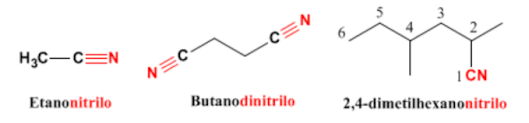
- Se nombran añadiendo la terminación -nitrilo al nombre del hidrocarburo de igual numero de átomosde carbono. Al grupo -C (tres enlaces) N como sustituyente se le designa mediante el prefijo ciano-.
- Nitrilos como grupo funcional: se nombran terminando el nombre del alcano en -nitrilo (metanonitrilo, etanonitrilo, propanonitrilo).
- Grupo ciano unido a ciclos: los nitrilos que contienen un ciclo como cadena principal se nombran terminando en -carbonitrilo el nombre del cicloalcano.
- Nitrilo como sustituyente: cuando el nitrilo actúa como sustituyente se denomina ciano y precede al nombre de la molécula, ordenándose alfabéticamente con el resto de sustituyentes.
Derivados Nitrogenados delos Hidrocarburos.
Nitrocompuestos
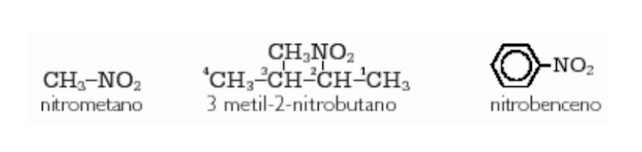
Los nitroderivados son compuestos cuyas moléculas poseen el grupo funcional nitro (–NO2).
• Los derivados aromáticos que poseen varios grupos nitro en la molécula secaracterizan por ser bastante inestables termodinámicamente, por lo que se utilizan como explosivos. Este grupo funcional siempre se considera un sustituyente del hidrogeno, por lo que se nombran anteponiendo el prefijo nitro- al nombre del hidrocarburo, indicando con un número su posición en la cadena carbonada.
Este grupo funcional siempre se considera un sustituyente del hidrogeno, por lo que se nombran anteponiendo el prefijo nitro- al nombre del hidrocarburo, indicando con un número su posición en la cadena carbonada.
¿DONDE SE ENCUENTRAN?
Dada la gran variedad de reacciones que sufren los nitrilos, son materia prima para un gran numero de compuestos de amplio uso en la industria y a nivel laboratorio. Excelente para elaborar todo tipo de empaques o bridas que contacten aceites, grasas o productos químicos diversos medianamente corrosivos.
Se utiliza en la producción de colorantes. Sirve para la producción de guantes de latex, para la industria química y farmacéutica. Se utiliza para la producción de esmaltes y pinturas. Productos de limpieza para uso industrial.
REFERENCIAS
E. (2011,
30 octubre). Aminas. Propiedades e Importancia – Química y
algo mas. https://quimicayalgomas.com/quimica-organica/aminas/
YouTube. (s. f.-b). Introducción a nomenclatura de aminas. Khan Academy. Recuperado 10 de
octubre de 2020, de https://www.youtube.com/watch?v=uUJAvcDXPfc&feature=youtu.be
U. (s. f.-g). NITRILOS. Nitrilos Características. Recuperado 10 de octubre de 2020, de http://funcionesnitrogenadas3013.blogspot.com/p/nutrilos. 1cidos%20correspondientes
.




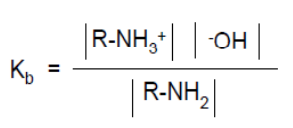


















No hay comentarios:
Publicar un comentario